Hubungi:Errol Zhou (Encik.)
Tel: tambah 86-551-65523315
Mudah Alih/WhatsApp: tambah 86 17705606359
QQ:196299583
Skype:lucytoday@hotmail.com
e-mel:sales@homesunshinepharma.com
Tambah:1002, Huanmao Bangunan, No.105, Mengcheng Jalan, Hefei Bandar, 230061, China
Chi-Med telah mengumumkan bahawa ia telah menerima Jawatankuasa agensi ubat Eropah (EMA) bagi produk perubatan untuk kegunaan manusia (CHMP) mengenai Sains surufatinib (juga dikenali sebagai HMPL-012 atau sulfatinib) dalam rawatan tumor (NET) yang maju (bersih) cadangkan.
Berdasarkan saranan CHMP, Chi-Med telah menyimpulkan: yang lengkap SANET-EP (non-pankreas NET) dan SANET-p (pankreas NET) kajian, dan status semasa Sofatinib dalam Non-pankreas dan pankreas di Amerika Syarikat terdapat data yang boleh membentuk asas untuk menyokong permohonan kebenaran pemasaran Eropah (MAA) untuk Sofatinib. Memandangkan hakikat bahawa tiada masalah pemfailan telah ditemui, selepas mengemukakan permohonan ubat baru (NDA) kepada Amerika Syarikat makanan dan pentadbiran dadah (FDA), ia dirancang untuk menghantar MAA di EU pada tahun 2021.
Sofatinib adalah satu jenis baru penindas yang tirosin oral (TKI) yang dibangunkan secara bebas oleh Chi-Med, yang mempunyai aktiviti dwi daripada anti-angiogenesis dan pengawalseliaan imun. Sofatinib boleh menghalang tumor angiogenesis dengan menghalang penerima faktor pertumbuhan (VEGFR) dan penerima faktor pertumbuhan (FGFR), dan boleh menghalang tanah jajahan merangsang faktor-1 penerima (i-1R). Dengan mengawal atur makro yang berkaitan dengan tumor, ia menggalakkan tindakbalas imun badan terhadap sel tumor. Kerana mekanisme yang unik daripada angiogenesis dan peraturan imun anti-tumor, Sofatinib mungkin sangat sesuai untuk digunakan dalam kombinasi dengan imunoterapies lain. Chi-Med kini memiliki semua hak Sofantinib di seluruh dunia.
Di China, Sofatinib telah mengemukakan dua aplikasi pemasaran ubat baru, dan merancang untuk dipasarkan buat pertama kalinya di China pada akhir 2020 untuk rawatan tumor neuroendokrin (bersih): (1) bukan pankreas NET aplikasi pemasaran ubat baru telah membuat kemajuan berasaskan SANET-keputusan positif daripada percubaan klinikal EP III telah dikemukakan pada akhir 2019. Pentadbiran produk perubatan Kebangsaan (NMPA) kini sedang dalam proses mengkaji semula permohonan pemasaran ubat baru. Chi-Med masih dijadualkan untuk dilancarkan pada akhir 2020. (2) permohonan pemasaran bagi ubat pankreas NET baru telah diserahkan-berikutan keputusan positif daripada percubaan klinikal SANET-p fasa III dan penamatan awal dalam analisis interim, Chi-Med telah mengemukakan permohonan pemasaran ubat baru Cina untuk rawatan pankreas NET, dan dijangka diterima dalam masa yang singkat.
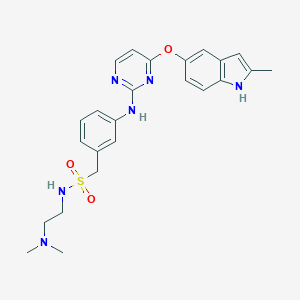
Struktur kimia surufatinib (sumber gambar: pubchem)
Chi-Med telah menubuhkan pasukan pengkomersilan onkologi sendiri dan bersedia untuk melancarkan ubat-ubatan onkologi baru yang akan datang. Pada separuh pertama 2020, Chi-Med mengesahkan strategi pendaftaran global untuk Sofatinib. Di Amerika Syarikat, permohonan pemasaran ubat baru dadah dalam penyediaan, dan ia dirancang untuk dikemukakan dengan bergolek penyerahan dari akhir 2020 hingga awal 2021, dan sedang bersedia untuk pelancaran ubat baru di Amerika Syarikat pada akhir 2021. Di Eropah, pelan Chi-Med untuk mengemukakan permohonan kebenaran pemasaran bersih (MAA) pada 2021.
Pada Julai 30, Chi-Med mengumumkan "2020 keputusan interim dan kemajuan terkini projek klinikal utama", yang juga termasuk kemajuan yang relevan dalam kerjasama klinikal Sofantinib:
---Terapi kombinasi dengan Tuoyi® memasuki percubaan klinikal Fasa II: a Fasa II ujian klinikal Sofatinib digabungkan dengan Tuoyi® (PD-1 monoclonal anti badan yang diluluskan oleh Junshi Biologics di China) untuk rawatan 8 tumor pepejal perbicaraan akan bermula pada awal 2020. Data yang diterbitkan di Persatuan Amerika untuk Penyelidikan Kanser ("AACR") menunjukkan bahawa terapi kombinasi yang baik diterima dan telah menunjukkan keberkesanan yang menggalakkan. Keberkesanan dos yang disyorkan ("RP2D") dalam ujian klinikal Fasa II boleh dinilai para pesakit adalah 64%, dan DCR adalah 100%.
—-Permulaan penyelidikan mengenai terapi kombinasi dengan daboshu® PD-1: pada Julai 2020, inovent melancarkan soventinib dan daboshu® (PD-1 monoclonal antibodi yang diluluskan oleh inovent di China) fasa I klinikal ujian gabungan terapi.
—-Bekerjasama dengan BeiGene Co., Ltd. ("BeiGene") untuk global PD-1: memulakan kerjasama pembangunan klinikal di Amerika Syarikat pada Mei 2020 untuk meneroka sofantinib dan tislelizumab (yang BeiGene PD-1 antibody) terapi kombinasi.